Reazioni chimiche di trasformare molecole in molecole diverse. Fanno così dall'interazione degli elettroni più esterno degli atomi interessati. Ci sono milioni di reazioni chimiche, ma principi sottostanti consentono di capirne il senso.
Calotta esterna
La calotta esterna di elettroni è la parte di un atomo che è impegnato in reazioni chimiche. Molecole sono spinti a reagire in modo tale da completare come il guscio esterno molti atomi come possibile, perché massimizza stabilità.
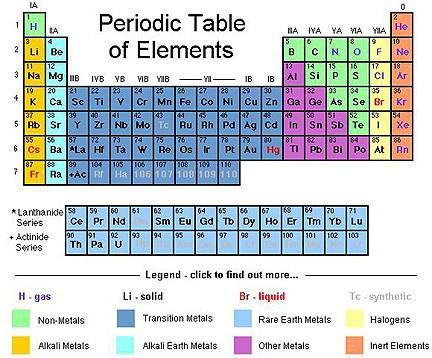
Tavola periodica
Il motivo di completare il guscio esterno è visto nella struttura della tavola periodica. Ad esempio, i gas nobili nella colonna di estrema destra sono chimicamente inerti, perché i loro gusci esterni sono pieni. Gli elementi appena sopra e appena sotto la posizione di sequenza di un gas nobile sono altamente reattivi con a vicenda.
Energia ed entropia
Reazioni più spontanee sono esotermiche, cioè, essi emanano più calore che assorbono. È simile a uno sciatore andando giù per una collina, dove l'energia potenziale gravitazionale è inferiore. L'unità per ottenere energia minima e massima entropia è ciò che motiva le reazioni chimiche.
Energia libera
L'interazione di queste due unità è la motivazione per l'invenzione di Willard Gibbs di "energia libera", un costrutto matematico che incorporano sia entropia e calore per analizzare più completamente spontaneità di reazione.
Acidi e basi
Un tipo importante di reazione chimica è neutralizzazione. Questo è quando un acido e base si combinano per neutralizzare l'altro. Reazioni di neutralizzazione producono generalmente un sale (molecola con un legame ionico) e acqua, un esempio può essere HCl(aq)+NaOH(aq) ' NaCl (aq) + H2O.