Solidi sono divisi in due categorie: solidi cristallini e solidi amorfi. Un solido cristallino ha un ordine a lungo raggio che è rigido. Gli esempi includono sale da tavola e ghiaccio. Solidi amorfi includono gomma, plastica e anche il vetro di cristallo, che è un termine improprio.
Rappresentazione
Sfere e bastoncini rappresentano gli atomi e molecole ripetute in cristalli. Il centro di ciascuna delle loro posizioni si chiama un "punto della grata".
Celle unitarie
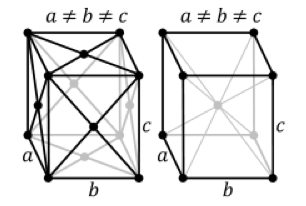
La struttura più piccola ripetuta in un cristallo è chiamata una "cella unitaria". Ci sono sette tipi, a seconda di quanti dell'unità sono uguali i lati della cella e quanti degli angoli dei lati sono angoli retti.
Centraggio
Una sfera può essere centrata nella cella unitaria. Ad esempio, in una cella cubica, una sfera (punto della grata) può sedersi al centro (chiamato "body-centered") o sei sfere possono sedersi al centro delle sei facce (chiamato "face-centered").
Forze
Le forze responsabili per la stabilità di un cristallo di eseguire l'intera gamma, da covalente e ionico (che legano le molecole) a forze di Van der Waals. Ad esempio, nel ghiaccio le molecole di H2O sono tenute insieme da forze di Van der Waals.
Efficienza di imballaggio
Efficienza di imballaggio è il rapporto tra occupati allo spazio non occupato in una cella unitaria. Ad esempio, forma cubica di NaCl ha un'efficienza di imballaggio del 52%, ma più stabile forma esagonale di zinco ha efficienza pari al 74% di imballaggio.