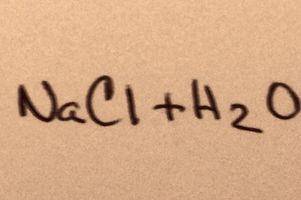Le nozioni di base
Quando un sale è aggiunto all'acqua, si scioglie nelle sue molecole componente fino a come molti ioni di sale come l'acqua, che sono in giro le molecole di idrogeno e ossigeno. Quando questo accade, la soluzione è "saturo". Come più sale è dissolto, ioni sodio e cloro urtano e ri-uniscono in cristalli di sale. Questo evento viene chiamato "precipitazione" perché il solido che si forma cade alla parte inferiore dell'acqua. Sali sono "idrofili," significato che essi sono attratti da acqua. Questa attrazione facilita un tipo più familiare di precipitazione; forma di gocce di pioggia nei dintorni di minuti cristalli di sale in nubi, dando pioggia sapore leggermente salato.
Elettroliti
Sale non condotta l'elettricità particolarmente bene allo stato solido, ma allo stato fuso (liquido), forme di sale una soluzione che può condurre elettricità abbastanza bene. Effettiva conducibilità dipende quali il sale viene utilizzato, ma questi liquidi, chiamati soluzioni elettrolitiche sono vettori convenienti per composti necessari per l'organismo umano. Impulsi elettrici generati dal cervello producono ossigeno libero, che viene utilizzato dal sangue. Le molecole di sale sono separate in elettroliti (sodio, potassio o calcio) e cloruri in soluzione: il cloro viene espulsa attraverso il sangue e reni nelle urine e gli elettroliti sono distribuiti in tutto il sistema neuro-muscolare in un processo che gli atleti sanno come re-idratazione.
Proprietà colligative
Qualsiasi soluzione si differenzia dalla sua composizione originale perché l'aggiunta di molecole, anche quando essi non si formano nuovi composti, cambia il peso molecolare del liquido e influisce sulle sue proprietà. Acqua salata è più densa di acqua fresca e si blocca più lentamente. Quando l'acqua congela, però, il sale migra verso il liquido circostante, rendendolo più pesante, più saturi, ulteriormente abbassare il suo punto di congelamento. A altra estremità dello spettro di materia, l'acqua salata più densa richiede più calore per trasformarla in un gas ma ancora lascia la maggior parte del sale dietro Man mano che evapora, rendendo un liquido più denso. Come la concentrazione di sale aumenta nel liquido, esso richiede più calore per far evaporare fino a quando finalmente l'acqua è andato, lasciando uno strato di sale in una padella rovente. Cuochi di attendere per aggiungere sale a un bollitore fino a quando l'acqua sta bollendo attivamente per lasciar calore nell'acqua così il sale non si ferma all'ebollizione. Queste qualità, chiamate "proprietà colligative," aiutano gli scienziati a determinare il peso molecolare dell'acqua salata. Se la massa del liquido, la pressione atmosferica e punto di ebollizione del liquido può essere stabilita, gli scienziati possono sottrarre il peso molecolare dell'acqua per trovare fuori che i sali sono presenti.